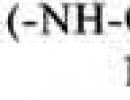Аминокислоты - структурные мономеры белков. Аминокислоты Аминокислоты и белки химические свойства
Предмет и задачи биологической химии. Биохимия как молекулярный уровень
изучения структурной организации, анаболизма и катаболизма живой материи.
Значение биохимии в подготовке врача.
Биологическая химия (биохимия) - это наука, изучающая химический состав живых организмов, превращения веществ и энергии, лежащей в основе их жизнедеятельности. Совокупность этих превращений составляет биологический обмен веществ, который является основой той формы движения материи, которую мы называем жизнью.
Живые организмы обладают необычными свойствами, отсутствующими в скоплении неживых молекул. К ним относятся следующие свойства: 1.1 Сложность и высокая степень организованности. Живые организмы представлены миллионами разных видов. 1.2 Любая составная часть организма имеет специальное назначение и выполняется строго определенную функцию. Это относится даже к индивидуальным химическим соединениям (липиды, белки и т.п.). 1.3Способность извлекать, преобразовывать и использовать энергию окружающей их среды – либо в форме органических питательных веществ, либо в виде энергии солнечного излучения Обмен веществ слагается из множества отдельных химических реакций, протекающих в живом организме и теснейшим образом связанных друг с другом. Данные экспериментальной биохимии свидетельствуют о взаимосвязи и неразрывности процесса поглощения и усвоения питательных веществ –ассимиляции и процесса их разложения и выделения – диссимиляции. Сопряженность и взаимосвязь отдельных реакций, происходящих при ассимиляции и диссимиляции питательных веществ в организме, проявляется также в сопряженности превращений энергии, происходящих в течение всей жизни организма.
1.4 Способность к точному самовоспроизведению. Цель биохимии состоит в том, чтобы понять, каким образом взаимодействия биомолекул друг с другом порождают описанные выше особенности живого состояния.
Биохимию разделяют на: 3.1 Статическую, изучающую химический состав живой материи; 3.2 Динамическую, изучающую процессы обмена веществ в организме; 3.3 Функциональную, изучающую процессы, лежащие в основе определенных проявлений жизнедеятельности. Первая часть обычно именуется органической химией и излагается в специальном курсе, вторая и третья части являются собственно биохимией.
Биологическая химия изучает молекулярные процессы, лежащие в основе развития и функционирования организмов. Биохимия использует методы «молекулярных» наук - химии, физической химии, молекулярной физики, и в этом отношении биохимия сама является молекулярной наукой.
Однако главные конечные задачи биохимии лежат в области биологии: она изучает закономерности биологической, а не химической формы движения материи. С другой стороны, «молекулярные изобретения» природы, открываемые биохимиками, находят применение в небиологических отраслях знания и в промышленности (молекулярная бионика, биотехнология). В таких случаях биохимия выступает в роли метода, а предметом исследований и разработок являются проблемы, выходящие за пределы биологии. Место биохимии как молекулярного уровня биологических исследований. Уровни исследования являются отражением уровней структурной организации биологических систем, образующих иерархический ряд от наиболее простых систем (молекулы организмов, молекулярный уровень) до предельно сложной земной биологической системы (биосферный уровень). Действительные связи между отраслями биологии гораздо сложнее, чем можно представить с помощью таких простых схем. В частности, каждый более простой уровень организации живых систем (и, соответственно, уровень их исследования) является частью более сложных уровней. Самый первый уровень - молекулярный - уникален в том отношении, что он является составной частью систем всех других уровней биологии. Соответственно этому выделяют такие разделы биохимии, как, например, молекулярная генетика, биохимическая экология. Высший уровень - биосферный - включает в себя все другие уровни.
Значение биохимических исследований.
Из определения биологической химии вытекает, что это химия живых существ. Живая система от неживой отличается обменом веществ и энергии (метаболизмом).
В результате обмена веществ (метаболизма) в биологические внутренние среды нашего организма поступает большое количество продуктов обмена веществ (метаболитов), содержание которых у здорового человека варьирует незначительно и составляет гомеостаз внутренних сред организма (кровь, сыворотка, спинномозговая жидкость, моча, пищеварительные соки и др.).
Практически любое заболевание начинается с повреждения (нарушения) одной реакции в метаболизме клетки, а затем оно распространяется на ткань, орган и целый организм. Нарушение метаболизма ведет к нарушению гомеостаза в биологических жидкостях организма человека, что сопровождается изменением биохимических показателей.
Большое значение клинико-биохимических методов исследования биологических жидкостей велико в медицине и важно для подготовки медицинских лабораторных техников. Достаточно напомнить, что только в крови человека можно определить современными методами биохимических исследований около 1000 показателей метаболизма.
Биохимические показатели биологических сред организма человека широко используются при:
1. постановке диагноза заболевания, особенно дифференциального диагноза;
2. выборе метода лечения;
3.контроле за правильностью назначенного лечения;
4.результаты биохимических анализов служат одним из критериев излеченности патологического процесса;
5.скрининге (выявлении болезни на доклинической стадии);
6.мониторинге (контроле за течением заболевания и результатом лечения);
7. прогнозе (информации о возможном исходе заболевания).
Бурный рост биохимии привел к тому, что она подразделилась на разные отрасли: клиническую биохимию, молекулярную биохимию, биохимию спорта и биохимию человека.
В процессе освоения дисциплины «Основы биохимии с методами клинико-биохимических исследований» перед нами встают задачи медицинской биохимии , заключающиеся в изучении:
1. строения и функций биомолекул, входящих в состав тканей организма.
2. механизмов:
· поступления пластических и биологически активных веществ во внутреннюю среду организма;
· превращения поступивших мономеров в биополимеры, специфичные для данного организма;
· высвобождения, накопления и использования энергии в клетке;
· образования и выведения конечных продуктов распада веществ в организме;
· воспроизведения и передачи наследственных признаков организма;
· регуляции всех перечисленных процессов.
Основное внимание нашего курса будет уделяться изучению методов клинико-биохимических исследований, которые состоят из этапов.
2 Аминокислоты, входящие в состав белков, их строение и свойства. Биологическая
роль аминокислот. Пептиды.
Белки - полимерные молекулы, в которых мономерами служат аминокислоты. В белках человека встречают только 20-АК.
А. Строение и свойства аминокислот
1. Общие структурные особенности аминокислот, входящих в состав белков
Общая структурная особенность АК - наличие амино- и карбоксильной групп, соединённых с одним и тем же углеродным атомом. R - радикал аминокислот - в простейшем случае представлен атомом водорода (глицин), но может иметь и более сложное строение.
В водных растворах при нейтральном значении рН - АК существуют в виде биполярных ионов.
В отличие от 19 остальных - АК, пролин - Иминокислота, радикал которой связан как с углеродным атомом, так и с аминогруппой, в результате чего молекула приобретает циклическую структуру.
19 из 20 АК содержат в α-положении асимметричный атом углерода, с которым связаны 4 разные замещающие группы. В результате эти АК в природе могут находиться в двух разных изомерных формах - L и D. Исключение составляет глицин, который не имеет асимметричного α-углеродного атома, так как его радикал представлен только атомом водорода. В составе белков присутствуют только L-изомеры аминокислот.
Чистые L- или D-стереоизомеры могут за длительный срок самопроизвольно и неферментатив-но превращаться в эквимолярную смесь L- и D-изомеров. Этот процесс называют рацемизацией. Рацемизация каждой L-аминокислоты при данной температуре идёт с определённой скоростью. Это обстоятельство можно использовать для установления возраста людей и животных. Так, в твёрдой эмали зубов имеется белок дентин, в котором L-аспартат переходит в D-изомер при температуре тела человека со скоростью 0,01% в год. В период формирования зубов в дентине содержится только L-изомер, поэтому по содержанию D-аспартата можно рассчитать возраст обследуемого.
Все 20 АК в организме человека различаются по строению, размерам и физико-химическим свойствам радикалов, присоединённых к α-углеродному атому.
2. Классификация аминокислот по химическому строению радикалов
По химическому строению АК можно разделить на алифатические, ароматические и гетероциклические.
В
составе алифатических радикалов могут
находиться функциональные группы,
придающие им специфические свойства:
карбоксильная (-СООН), амино (-NH 2),
тиольная (-SH), амидная (-CO-NH 2),
гидроксильная (-ОН) и гуанидиновая![]() группы.
группы.
Названия аминокислот можно построить по заместительной номенклатуре, но обычно используют тривиальные названия.
3. Классификация аминокислот по растворимости их радикалов в воде
АК с неполярными R : радикалы, имеющие алифатические углеводородные цепи (радикалы ала, вал, лей, изо, про и мет) и ароматические кольца (радикалы фен и три).
АК с полярными незаряженными R : эти радикалы лучше, чем гидрофобные радикалы, растворяются в воде, т.к. в их состав входят полярные функциональные группы, образующие водородные связи с водой. К ним относят сер, тре и тир, имеющие гидроксильные группы, асн и глн, содержащие амидные группы, и цис с его тиольной группой.
Цистеин и тирозин содержат соответственно тиольную и гидроксильную группы, способные к диссоциации с образованием Н + , но при рН около 7,0, поддерживаемого в клетках, эти группы практически не диссоциируют.
АК с полярными отрицательно заряженными R : о тносят асн и глн аминокислоты, имеющие в радикале дополнительную карбоксильную группу, при рН около 7,0 диссоциирующую с образованием СОО - и Н + . Следовательно, радикалы данных аминокислот - анионы. Ионизированные формы глутаминовой и аспарагиновой кислот называют соответственно глутаматом и аспартатом.
АК с полярными положительно заряженными R :
α-Аминокислоты могут ковалентно связываться друг с другом с помощью пептидных связей. Пептидная связь образуется между α-карбоксильной группой одной аминокислоты и α-аминогруппой другой, т.е. является амидной связью. При этом происходит отщепление молекулы воды.
1. Строение пептида. Количество аминокислот в составе пептидов может сильно варьировать. Пептиды, содержащие до 10 аминокислот, называют олигопептиды. Часто в названии таких молекул указывают количество входящих в состав олигопептида аминокислот: трипептид, пентапептид, окгапептид и т.д.
Пептиды, содержащие более 10 аминокислот, называют "полипептиды", а полипептиды, состоящие из более чем 50 аминокислотных остатков, обычно называют белками. Однако эти названия условны, так как термин "белок" часто употребляют для обозначения полипептида, содержащего менее 50 аминокислотных остатков. Например, гормон глюкагон, состоящий из 29 аминокислот, называют белковым гормоном.
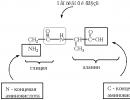
Мономеры аминокислот, входящих в состав белков, называют "аминокислотные остатки". Аминокислотный остаток, имеющий свободную аминогруппу, называется N-концевым и пишется слева, а имеющий свободную α-карбоксильную группу - С-концевым и пишется справа. Пептиды пишутся и читаются с N-конца. Цепь повторяющихся атомов в полипептидной цепи -NH-CH-CO-носит название "пептидный остов" .
При названии полипептида к сокращённому названию аминокислотных остатков добавляют суффикс -ил, за исключением С-концевой аминокислоты. Например, тетрапептид Сер-Гли-Про-Ала читается как серилглицилпролилаланин.
Пептидная связь, образуемая иминогруппой пролина, отличается от других пептидных связей, так как атом азота пептидной группы связан не с водородом, а с радикалом.
Пептиды различаются по аминокислотному составу, количеству и порядку соединения аминокислот

3 Первичная структура белков. Пептидная связь, ее характеристика (прочность, кратность, компланарность, цис- ,транс- изомерия). Значение первичной структуры для нормального функционирования белков (на примере гемоглобина S).
Первичная структура - понятие, обозначающее последовательность аминокислотных остатков в белке Пептидная связь - основной вид связи, определяющий первичную структуру Возможно и присутствие дисульфидных связей между двумя остатками цистеина в одной полипептидной цепи с образованием цистина Такая же связь (дисульфидный мостик) может возникать и между остатками цистеина, принадлежащими разным полипептидным цепям в белковой молекуле, сополимерном образовании.
Аминокислотные остатки в пептидной цепи белков чередуются не случайным образом, а расположены в определённом порядке. Линейную последовательность аминокислотных остатков в полипептидной цепи называют "первичная структура белка".
Первичная структура каждого индивидуального белка закодирована в участке ДНК, называемом геном. В процессе синтеза белка информация, находящаяся в гене, сначала переписывается на мРНК, а затем, используя мРНК в качестве матрицы, на рибосоме происходит сборка первичной структуры белка.
Каждый из 50 000 индивидуальных белков организма человека имеет уникальную для данного белка первичную структуру. Все молекулы данного индивидуального белка имеют одинаковое чередование аминокислотных остатков в белке, что в первую очередь отличает данный индивидуальный белок от любого другого
Аминокислотами называются органические карбоновые кислоты, у которых как минимум один из атомов водорода углеводородной цепи замещен на аминогруппу. В зависимости от положения группы -NН 2 различают α, β, γ и т. д. L-аминокислоты. К настоящему времени в различных объектах живого мира найдено до 200 различных аминокислот. В организме человека содержится около 60 различных аминокислот и их производных, но не все они входят в состав белков.
Аминокислоты делятся на две группы:
- протеиногенные (входящие в состав белков)
Среди них выделяют главные (их всего 20) и редкие. Редкие белковые аминокислоты (например, гидроксипролин, гидроксилизин, аминолимонная кислота и др.) на самом деле являются производными тех же 20 аминокислот.
Остальные аминокислоты не участвуют в построении белков; они находятся в клетке либо в свободном виде (как продукты обмена), либо входят в состав других небелковых соединений. Например, аминокислоты орнитин и цитруллин являются промежуточными продуктами в образовании протеиногенной аминокислоты аргинина и участвуют в цикле синтеза мочевины; γ-амино-масляная кислота тоже находится в свободном виде и играет роль медиатора в передаче нервных импульсов; β-аланин входит в состав витамина - пантотеновой кислоты.
- непротеиногенные (не участвующие в образовании белков)
Непротеиногенные аминокислоты в отличие от протеиногенных более разнообразны, особенно те, которые содержатся в грибах, высших растениях. Протеиногенные аминокислоты участвуют в построении множества разных белков независимо от вида организма, а непротеиногенные аминокислоты могут быть даже токсичны для организма другого вида, т. е. ведут себя как обычные чужеродные вещества. Например, канаванин, дьенколевая кислота и β-циано-аланин, выделенные из растений, ядовиты для человека.
Строение и классификация протеиногенных аминокислот
Радикал R в простейшем случае представлен атомом водорода (глицин), а может иметь и сложное строение. Поэтому α-аминокислоты отличаются друг от друга прежде всего строением бокового радикала, а следовательно, и физико-химическими свойствами, присущими этим радикалам. Приняты три классификации аминокислот:
Приведенная физиологическая классификация аминокислот не универсальна в отличие от первых двух классификаций и до некоторой степени условна, поскольку действительна только для организмов данного вида. Однако абсолютная незаменимость восьми аминокислот универсальна для всех видов организмов (в табл. 2 приведены данные для некоторых представителей позвоночных и насекомых [показать] ).
| Таблица 2. Незаменимые (+), заменимые (-) и полузаменимые (±) аминокислоты для некоторых позвоночных и насекомых (по Любке и др., 1975) | |||||||
| Аминокислоты | Человек | Крыса | Мышь | Курица | Лосось | Москит | Пчела |
| Глицин | - | - | - | + | - | + | - |
| Алании | - | - | - | - | - | - | - |
| Валин | + | + | + | + | + | + | + |
| Лейцин | + | + | + | + | + | + | + |
| Изолейцин | + | + | + | + | + | + | + |
| Цистеин | - | - | - | - | - | - | - |
| Метионин | + | + | + | + | + | + | + |
| Серин | - | - | - | - | - | - | - |
| Треонин | + | + | + | + | + | + | + |
| Аспарагиновая кислота | - | - | - | - | - | - | - |
| Глутаминовая кислота | - | - | - | - | - | - | - |
| Лизин | + | + | + | + | + | + | + |
| Аргинин | ± | ± | + | + | + | + | + |
| Фенилаланин | + | + | + | + | + | + | + |
| Тирозин | ± | ± | + | + | - | - | - |
| Гистидин | ± | + | + | + | + | + | + |
| Триптофан | + | + | + | + | + | + | + |
| Пролин | - | - | - | - | - | - | - |
Для крыс и мышей незаменимых аминокислот уже девять (к восьми известным добавляется гистидин). Нормальный рост и развитие курицы возможны только при наличии одиннадцати незаменимых аминокислот (добавляются гистидин, аргинин, тирозин), т. е. полузаменимые для человека аминокислоты абсолютно незаменимы для курицы. Для москитов глицин является абсолютно незаменимой, а тирозин, наоборот, заменимой аминокислотой.
Значит, для разных видов организмов возможны существенные отклонения в потребности в отдельных аминокислотах, что определяется особенностями их обмена.
Сложившийся для каждого вида организма состав незаменимых аминокислот, или так называемая ауксотрофность организма в отношении аминокислот, отражает скорее всего стремление его к минимальным энергетическим затратам на синтез аминокислот. Действительно, выгоднее получать готовый продукт, чем производить его самому. Поэтому организмы, потребляющие незаменимые аминокислоты, тратят примерно на 20% энергии меньше, чем те, которые синтезируют все аминокислоты. С другой стороны, в ходе эволюции не сохранилось таких форм жизни, которые бы полностью зависели от поступления всех аминокислот извне. Им трудно было бы приспосабливаться к изменениям внешней среды, учитывая, что аминокислоты являются материалом для синтеза такого вещества, как белок, без которого жизнь невозможна.
Физико-химические свойства аминокислот
Кислотно-основные свойства аминокислот . По химическим свойствам аминокислоты - амфотерные электролиты, т. е. сочетают свойства и кислот, и оснований.

Кислотные группы аминокислот: карбоксильная (-СООН -> -СОО - + Н +), протонированная α-аминогруппа (-NH + 3 -> -NН 2 + Н +).
Основные группы аминокислот: диссоциированная карбоксильная (-СОО - + Н + -> -СООН) и α-аминогруппа (-NН 2 + Н + -> NН + 3).
Для каждой аминокислоты имеется как минимум две константы кислотной диссоциации рК а - одна для группы -СООН, а вторая для α-аминогруппы.
В водном растворе возможно существование трех форм аминокислот (рис. 1.)
Доказано, что в водных растворах аминокислоты находятся в виде диполя; или цвиттер-иона.
Влияние рН среды на ионизацию аминокислот . Изменение рН среды от кислой до щелочной влияет на заряд растворенных аминокислот. В кислой среде (рН<7) все аминокислоты несут положительный заряд (существуют в виде катиона), так как избыток протонов в среде подавляет диссоциацию карбоксильной группы:

В кислой среде аминокислоты в электрическом поле движутся к катоду.
В щелочной среде (рН>7), где имеется избыток ионов ОН - , аминокислоты находятся в виде отрицательно заряженных ионов (анионов), так как диссоциирует NН + 3 -группа:
В этом случае аминокислоты перемещаются в электрическом поле к аноду.
Следовательно, в зависимости от рН среды аминокислоты имеют суммарный нулевой, положительный или отрицательный заряд.
Состояние, в котором заряд аминокислоты равен нулю, называется изоэлектрическим. Значение рН, при котором наступает такое состояние и аминокислота не перемещается в электрическом поле ни к аноду, ни к катоду, называется изоэлектрической точкой и обозначается рН I . Изоэлектрическая точка очень точно отражает кислотно-основные свойства разных групп в аминокислотах и является одной из важных констант, характеризующих аминокислоту.
Изоэлектрическая точка неполярных (гидрофобных) аминокислот приближается к нейтральному значению рН (от 5,5 для фенилаланина до 6,3 для пролина), у кислых она имеет низкие значения (для глутаминовой кислоты 3,2, для аспарагиновой 2,8). Изоэлектрическая точка для цистеина и цистина равна 5,0, что указывает на слабые кислотные свойства этих аминокислот. У основных аминокислот - гистидина и особенно лизина и аргинина - изоэлектрическая точка значительно выше 7.
В клетках и межклеточной жидкости организма человека и животных рН среды близка к нейтральной, поэтому основные аминокислоты (лизин, аргинин) несут суммарный положительный заряд (катионы), кислые аминокислоты (аспарагиновая и глутаминовая) имеют отрицательный заряд (анионы), а остальные существуют в виде диполя. Кислые и основные аминокислоты больше гидратированы, чем все остальные аминокислоты.
Стереоизомерия аминокислот
Все протеиногенные аминокислоты, за исключением глицина, имеют как минимум один асимметрический атом углерода (С*) и обладают оптической активностью, причем большая часть их относится к левовращающим. Они существуют в виде пространственных изомеров, или стереоизомеров. По расположению заместителей вокруг асимметрического атома углерода стерео-изомеры относят к L- или D-ряду.
L- и D-изомеры относятся друг к другу как предмет и его зеркальное изображение, поэтому их называют также зеркальными изомерами или энантиомерами. Аминокислоты треонин и изолейцин имеют по два асимметрических атома углерода, поэтому у них по четыре стереоизомера. Например, у треонина, помимо L- и D-треонина, имеется еще два, которые называют диастереомерами или аллоформами: L-аллотреонин и D-аллотреонин.
Все аминокислоты, входящие в состав белков, относятся к L-ряду. Считалось, что D-аминокислоты не встречаются в живой природе. Однако были найдены полипептиды в виде полимеров D-глутаминовой кислоты в капсулах спороносных бактерий (палочке сибирской язвы, картофельной и сенной палочке); D-глутаминовая кислота и D-аланин входят в состав мукопептидов клеточной стенки некоторых бактерий. D-Аминокислоты обнаружены также в антибиотиках, продуцируемых микроорганизмами (см. табл. 3).
Возможно, D-аминокислоты оказались более пригодными для защитных функций организмов (именно этой цели служат и капсула бактерий, и антибиотики), в то время как L-аминокислоты нужны организму для построения белков.
Распространение отдельных аминокислот в разных белках
К настоящему времени расшифрован аминокислотный состав многих белков микробного, растительного и животного происхождения. Наиболее часто в белках находят аланин, глицин, лейцин, серии. Однако каждый белок имеет свой аминокислотный состав. Например, протамины (простые белки, находящиеся в молоках рыб) содержат до 85% аргинина, но в них отсутствуют циклические, кислые и серусодержащие аминокислоты, треонин и лизин. Фиброин - белок натурального шелка, содержит до 50% глицина; в состав коллагена - белка сухожилий - входят редкие аминокислоты (гидроксилизин, гидроксипролин), которые отсутствуют в остальных белках.
Аминокислотный состав белков определяется не доступностью или незаменимостью той или иной аминокислоты, а назначением белка, его функцией. Последовательность расположения аминокислот в белке обусловлена генетическим кодом.
| Страница 2 | всего страниц: 7 |
Среди азотсодержащих органических веществ имеются соединения с двойственной функцией. Особенно важными из них являются аминокислоты .
В клетках и тканях живых организмов встречается около 300 различных аминокислот, но только 20 ( α-аминокислоты) из них служат звеньями (мономерами), из которых построены пептиды и белки всех организмов (поэтому их называют белковыми аминокислотами). Последовательность расположения этих аминокислот в белках закодирована в последовательности нуклеотидов соответствующих генов. Остальные аминокислоты встречаются как в виде свободных молекул, так и в связанном виде. Многие из аминокислот встречаются лишь в определенных организмах, а есть и такие, которые обнаруживаются только в одном из великого множества описанных организмов. Большинство микроорганизмов и растения синтезируют необходимые им аминокислоты; животные и человек не способны к образованию так называемых незаменимых аминокислот, получаемых с пищей. Аминокислоты участвуют в обмене белков и углеводов, в образовании важных для организмов соединений (например, пуриновых и пиримидиновых оснований, являющихся неотъемлемой частью нуклеиновых кислот), входят в состав гормонов, витаминов, алкалоидов, пигментов, токсинов, антибиотиков и т. д.; некоторые аминокислоты служат посредниками при передаче нервных импульсов.
Аминокислоты - органические амфотерные соединения, в состав которых входят карбоксильные группы – СООН и аминогруппы -NH 2 .
Аминокислоты можно рассматривать как карбоновые кислоты, в молекулах которых атом водорода в радикале замещен аминогруппой.
КЛАССИФИКАЦИЯ
Аминокислоты классифицируют по структурным признакам.1. В зависимости от взаимного расположения амино- и карбоксильной групп аминокислоты подразделяют на α-, β-, γ-, δ-, ε- и т. д.
2. В зависимости от количества функциональных групп различают кислые, нейтральные и основные.
3. По характеру углеводородного радикала различают алифатические (жирные), ароматические, серосодержащие и гетероциклические аминокислоты. Приведенные выше аминокислоты относятся к жирному ряду.
Примером ароматической аминокислоты может служить пара -аминобензойная кислота:
Примером гетероциклической аминокислоты может служить триптофан –незаменимая α- аминокислота
НОМЕНКЛАТУРА
По систематической номенклатуре названия
аминокислот образуются из названий соответствующих кислот прибавлением
приставки амино-
и указанием места расположения аминогруппы по отношению
к карбоксильной группе. Нумерация углеродной цепи с атома углерода карбоксильной группы.
Например:
Часто используется также другой способ построения названий аминокислот, согласно которому к тривиальному названию карбоновой кислоты добавляется приставка амино- с указанием положения аминогруппы буквой греческого алфавита.
Пример:
Для α-аминокислот R-CH(NH 2)COOH
Которые играют исключительно важную роль в процессах жизнедеятельности животных и растений, применяются тривиальные названия.
Таблица.
|
Аминокислота |
Сокращённое обозначение |
Строение радикала (R) |
|
Глицин |
Gly (Гли) |
H - |
|
Аланин |
Ala (Ала) |
CH 3 - |
|
Валин |
Val (Вал) |
(CH 3) 2 CH - |
|
Лейцин |
Leu (Лей) |
(CH 3) 2 CH – CH 2 - |
|
Серин |
Ser (Сер) |
OH- CH 2 - |
|
Тирозин |
Tyr (Тир) |
HO – C 6 H 4 – CH 2 - |
|
Аспарагиновая кислота |
Asp (Асп) |
HOOC – CH 2 - |
|
Глутаминовая кислота |
Glu (Глу) |
HOOC – CH 2 – CH 2 - |
|
Цистеин |
Cys (Цис) |
HS – CH 2 - |
|
Аспарагин |
Asn (Асн) |
O = C – CH 2 – │ NH 2 |
|
Лизин |
Lys (Лиз) |
NH 2 – CH 2 - CH 2 – CH 2 - |
|
Фенилаланин |
Phen (Фен) |
C 6 H 5 – CH 2 - |
Если в молекуле аминокислоты содержится две аминогруппы, то в ее названии используется приставка диамино- , три группы NH 2 – триамино- и т.д.
Пример:
Наличие двух или трех карбоксильных групп отражается в названии суффиксом –диовая или -триовая кислота :
ИЗОМЕРИЯ
1. Изомерия углеродного скелета
2. Изомерия положения функциональных групп
3. Оптическая изомерия
α-аминокислоты, кроме глицина NН 2 -CH 2 -COOH.
ФИЗИЧЕСКИЕ СВОЙСТВА
Аминокислоты представляют собой кристаллические вещества с высокими (выше 250°С) температурами плавления, которые мало отличаются у индивидуальных аминокислот и поэтому нехарактерны. Плавление сопровождается разложением вещества. Аминокислоты хорошо растворимы в воде и нерастворимы в органических растворителях, чем они похожи на неорганические соединения. Многие аминокислоты обладают сладким вкусом.
ПОЛУЧЕНИЕ
3. Микробиологический синтез. Известны микроорганизмы, которые в процессе жизнедеятельности продуцируют α - аминокислоты белков.
ХИМИЧЕСКИЕ СВОЙСТВА
Аминокислоты амфотерные органические соединения, для них характерны кислотно-основные свойства.
I . Общие свойства
1. Внутримолекулярная нейтрализация → образуется биполярный цвиттер-ион:
Водные растворы электропроводны. Эти свойства объясняются тем, что молекулы аминокислот существуют в виде внутренних солей, которые образуются за счет переноса протона от карбоксила к аминогруппе:
цвиттер-ион
Водные растворы аминокислот имеют нейтральную, кислую или щелочную среду в зависимости от количества функциональных групп.
ПРИМЕНЕНИЕ
1) аминокислоты широко распространены в природе;
2) молекулы аминокислот – это те кирпичики, из которых построены все растительные и животные белки; аминокислоты, необходимые для построения белков организма, человек и животные получают в составе белков пищи;
3) аминокислоты прописываются при сильном истощении, после тяжелых операций;
4) их используют для питания больных;
5) аминокислоты необходимы в качестве лечебного средства при некоторых болезнях (например, глутаминовая кислота используется при нервных заболеваниях, гистидин – при язве желудка);
6) некоторые аминокислоты применяются в сельском хозяйстве для подкормки животных, что положительно влияет на их рост;
7) имеют техническое значение: аминокапроновая и аминоэнантовая кислоты образуют синтетические волокна – капрон и энант.
О РОЛИ АМИНОКИСЛОТ
Нахождение в природе и биологическая роль аминокислот
Нахождение в природе и би...гическая роль аминокислот
Белки составляют материальную основу химической деятельности клетки. Функции белков в природе универсальны. Названию белки, наиболее принятому в отечественной литературе, соответствует термин протеины (от греч. proteios - первый). К настоящему времени достигнуты большие успехи в установлении соотношения структуры и функций белков, механизма их участия в важнейших процессах жизнедеятельности организма и в понимании молекулярных основ патогенеза многих болезней.
В зависимости от молекулярной массы различают пептиды и белки. Пептиды имеют меньшую молекулярную массу, чем белки. Для пептидов более свойственна регуляторная функция (гормоны, ингибиторы и активаторы ферментов, переносчики ионов через мембраны, антибиотики, токсины и др.).
12.1. α -Аминокислоты
12.1.1. Классификация
Пептиды и белки построены из остатков α-аминокислот. Общее число встречающихся в природе аминокислот превышает 100, но некоторые из них обнаружены лишь в определенном сообществе орга- низмов, 20 наиболее важных α-аминокислот постоянно встречаются во всех белках (схема 12.1).
α-Аминокислоты - гетерофункциональные соединения, молекулы которых содержат одновременно аминогруппу и карбоксильную группу у одного и того же атома углерода.
Схема 12.1. Важнейшие α-аминокислоты*

* Сокращенные обозначения применяются только для записи аминокислотных остатков в молекулах пептидов и белков. ** Незаменимые аминокислоты.
Названия α-аминокислот могут быть построены по заместительной номенклатуре, но чаще используются их тривиальные названия.

Тривиальные названия α-аминокислот обычно связаны с источниками выделения. Серин входит в состав фиброина шелка (от лат. serieus - шелковистый); тирозин впервые выделен из сыра (от греч. tyros - сыр); глутамин - из злаковой клейковины (от нем. Gluten - клей); аспарагиновая кислота - из ростков спаржи (от лат. asparagus - спаржа).
Многие α-аминокислоты синтезируются в организме. Некоторые аминокислоты, необходимые для синтеза белков, в организме не образуются и должны поступать извне. Такие аминокислоты называют незаменимыми (см. схему 12.1).
К незаменимым α-аминокислотам относятся:
валин изолейцин метионин триптофан
лейцин лизин треонин фенилаланин
α-Аминокислоты классифицируют несколькими способами в зависимости от признака, положенного в основу их деления на группы.
Одним из классификационных признаков служит химическая природа радикала R. По этому признаку аминокислоты делятся на алифатические, ароматические и гетероциклические (см. схему 12.1).
Алифатические α-аминокислоты. Это наиболее многочисленная группа. Внутри нее аминокислоты подразделяют с привлечением дополнительных классификационных признаков.
В зависимости от числа карбоксильных групп и аминогрупп в молекуле выделяют:
Нейтральные аминокислоты - по одной группе NH 2 и СООН;
Основные аминокислоты - две группы NH 2 и одна группа
СООН;
Кислые аминокислоты - одна группа NH 2 и две группы СООН.
Можно отметить, что в группе алифатических нейтральных аминокислот число атомов углерода в цепи не бывает больше шести. При этом не существует аминокислоты с четырьмя атомами углерода в цепи, а аминокисоты с пятью и шестью атомами углерода имеют только разветвленное строение (валин, лейцин, изолейцин).
В алифатическом радикале могут содержаться «дополнительные» функциональные группы:
Гидроксильная - серин, треонин;
Карбоксильная - аспарагиновая и глутаминовая кислоты;
Тиольная - цистеин;
Амидная - аспарагин, глутамин.
Ароматические α-аминокислоты. К этой группе относятся фенилаланин и тирозин, построенные таким образом, что бензольные кольца в них отделены от общего α-аминокислотного фрагмента метиленовой группой -СН 2-.

Гетероциклические α-аминокислоты. Относящиеся к этой группе гистидин и триптофан содержат гетероциклы - имидазол и индол соответственно. Строение и свойства этих гетероциклов рассмотрены ниже (см. 13.3.1; 13.3.2). Общий принцип построения гетероциклических аминокислот такой же, как и ароматических.
Гетероциклические и ароматические α-аминокислоты можно рассматривать как β-замещенные производные аланина.

К героциклическим относится также аминокислота пролин, в которой вторичная аминогруппа включена в состав пирролидинового

В химии α-аминокислот большое внимание уделяется строению и свойствам «боковых» радикалов R, которые играют важную роль в формировании структуры белков и выполнении ими биологических функций. Большое значение имеют такие характеристики, как полярность «боковых» радикалов, наличие в радикалах функциональных групп и способность этих функциональных групп к ионизации.
В зависимости от бокового радикала выделяют аминокислоты с неполярными (гидрофобными) радикалами и аминокислоты c поляр- ными (гидрофильными) радикалами.
К первой группе относятся аминокислоты с алифатическими боковыми радикалами - аланин, валин, лейцин, изолейцин, метионин - и ароматическими боковыми радикалами - фенилаланин, триптофан.
Ко второй группе принадлежат аминокислоты, у которых в радикале имеются полярные функциональные группы, способные к иони- зации (ионогенные) или не способные переходить в ионное состояние (неионогенные) в условиях организма. Например, в тирозине гидроксильная группа ионогенная (имеет фенольный характер), в серине - неионогенная (имеет спиртовую природу).

Полярные аминокислоты с ионогенными группами в радикалах в определенных условиях могут находиться в ионном (анионном или катионном) состоянии.

12.1.2. Стереоизомерия
Основной тип построения α-аминокислот, т. е. связь одного и того же атома углерода с двумя разными функциональными группами, радикалом и атомом водорода, уже сам по себе предопределяет хираль- ность α-атома углерода. Исключение составляет простейшая аминокислота глицин H 2 NCH 2 COOH, не имеющая центра хиральности.
Конфигурация α-аминокислот определяется по конфигурационному стандарту - глицериновому альдегиду. Расположение в стандартной проекционной формуле Фишера аминогруппы слева (подобно группе ОН в l-глицериновом альдегиде) соответствует l-конфи- гурации, справа - d-конфигурации хирального атома углерода. По R, S-системе α-атом углерода у всех α-аминокислот l-ряда имеет S-, а у d-ряда - R-конфигурацию (исключение составляет цистеин, см. 7.1.2).
Большинство α-аминокислот содержит в молекуле один асимметрический атом углерода и существует в виде двух оптически активных энантиомеров и одного оптически неактивного рацемата. Почти все природные α-аминокислоты принадлежат к l-ряду.

Аминокислоты изолейцин, треонин и 4-гидроксипролин содержат в молекуле по два центра хиральности.

Такие аминокислоты могут существовать в виде четырех стереоизомеров, представляющих собой две пары энантиомеров, каждая из которых образует рацемат. Для построения белков животных организмов используется только один из энантиомеров.
Стереоизомерия изолейцина аналогична рассмотренной ранее стереоизомерии треонина (см. 7.1.3). Из четырех стереоизомеров в состав белков входит l-изолейцин с S-конфигурацией обоих асимметрических атомов углерода С-α и С-β. В названиях другой пары энантиомеров, являющихся диастереомерами по отношению к лейцину, используется приставка алло-.

Расщепление рацематов. Источником получения α-аминокислот l-ряда служат белки, которые подвергают для этого гидролитическому расщеплению. В связи с большой потребностью в отдельных энантиомерах (для синтеза белков, лекарственных веществ и т. п.) разработаны химические методы расщепления синтетических рацемических аминокислот. Предпочтителен ферментативный способ расщепления с использованием ферментов. В настоящее время для разделения рацемических смесей используют хроматографию на хиральных сорбентах.
12.1.3. Кислотно-основные свойства
Амфотерность аминокислот обусловлена кислотными (СООН) и основными (NH 2) функциональными группами в их молекулах. Аминокислоты образуют соли как со щелочами, так и с кислотами.
В кристаллическом состоянии α-аминокислоты существуют как диполярные ионы H3N+ - CHR-COO- (обычно используемая запись
строения аминокислоты в неионизированной форме служит лишь для удобства).
В водном растворе аминокислоты существуют в виде равновесной смеси диполярного иона, катионной и анионной форм.

Положение равновесия зависит от рН среды. У всех аминокислот преобладают катионные формы в сильнокислых (рН 1-2) и анион- ные - в сильнощелочных (рН >11) средах.
Ионное строение обусловливает ряд специфических свойств аминокислот: высокую температуру плавления (выше 200 ?С), растворимость в воде и нерастворимость в неполярных органических растворителях. Способность большинства аминокислот хорошо растворяться в воде является важным фактором обеспечения их биологического функционирования, с нею связаны всасывание аминокислот, их транспорт в организме и т. п.
Полностью протонированная аминокислота (катионная форма) с позиций теории Брёнстеда является двухосновной кислотой,
Отдавая один протон, такая двухосновная кислота превращается в слабую одноосновную кислоту - диполярный ион с одной кислотной группой NH 3 + . Депротонирование диполярного иона приводит к получению анионной формы аминокислоты - карбоксилат-иона, являющегося основанием Брёнстеда. Значения характеризую-
щие кислотные свойства карбоксильной группы аминокислот, обычно лежат в интервале от 1 до 3; значения рK а2 характеризующие кислотность аммониевой группы, - от 9 до 10 (табл. 12.1).
Таблица 12.1. Кислотно-основные свойства важнейших α-аминокислот

Положение равновесия, т. е. соотношение различных форм аминокислоты, в водном растворе при определенных значениях рН существенно зависит от строения радикала, главным образом от присутствия в нем ионогенных групп, играющих роль дополнительных кислотных и основных центров.
Значение рН, при котором концентрация диполярных ионов максимальна, а минимальные концентрации катионных и анионных форм аминокислоты равны, называется изоэлектрической точкой (p/).
Нейтральные α-аминокислоты. Эти аминокислоты имеют значения рI несколько ниже 7 (5,5-6,3) вследствие большей способности к ионизации карбоксильной группы под влиянием -/-эффекта группы NH 2 . Например, у аланина изоэлектрическая точка находится при рН 6,0.

Кислые α-аминокислоты. Эти аминокислоты имеют в радикале дополнительную карбоксильную группу и в сильнокислой среде находятся в полностью протонированной форме. Кислые аминокислоты являются трехосновными (по Брёндстеду) с тремя значениями рК а, как это видно на примере аспарагиновой кислоты (р/ 3,0).

У кислых аминокислот (аспарагиновой и глутаминовой) изоэлектрическая точка находится при рН много ниже 7 (см. табл. 12.1). В организме при физиологических значениях рН (например, рН крови 7,3-7,5) эти кислоты находятся в анионной форме, так как у них ионизированы обе карбоксильные группы.
Основные α-аминокислоты. В случае основных аминокислот изоэлектрические точки находятся в области рН выше 7. В сильно- кислой среде эти соединения также представляют собой трехосновные кислоты, этапы ионизации которых показаны на примере лизина (р/ 9,8).

В организме основные аминокислоты находятся в виде катионов, т. е. у них протонированы обе аминогруппы.
В целом ни одна α -аминокислота in vivo не находится в своей изоэлектрической точке и не попадает в состояние, отвечающее наименьшей растворимости в воде. Все аминокислоты в организме находятся в ионной форме.
12.1.4. Аналитически важные реакции α -аминокислот
α-Аминокислоты как гетерофункциональные соединения вступают в реакции, характерные как для карбоксильной, так и для аминогруппы. Некоторые химические свойства аминокислот обусловлены функциональными группами в радикале. В настоящем разделе рассматриваются реакции, имеющие практическое значение для идентификации и анализа аминокислот.
Этерификация. При взаимодействии аминокислот со спиртами в присутствии кислотного катализатора (например, газообразный хлороводород) с хорошим выходом получаются сложные эфиры в виде гидрохлоридов. Для выделения свободных эфиров реакционную смесь обрабатывают газообразным аммиаком.

Сложные эфиры аминокислот не имеют диполярного строения, поэтому, в отличие от исходных кислот, они растворяются в органических растворителях и обладают летучестью. Так, глицин - крис- таллическое вещество с высокой температурой плавления (292 ?С), а его метиловый эфир - жидкость с температурой кипения 130 ?С. Анализ эфиров аминокислот можно проводить с помощью газожидкостной хроматографии.
Реакция с формальдегидом. Практическое значение имеет реакция с формальдегидом, которая лежит в основе количественного определения аминокислот методом формольного титрования (метод Сёренсена).
Амфотерность аминокислот не позволяет проводить непосредственно титрование их щелочью в аналитических целях. При взаимодействии аминокислот с формальдегидом получаются относительно устойчивые аминоспирты (см. 5.3) - N-гидроксиметильные производные, свободную карбоксильную группу которых затем титруют щелочью.
Качественные реакции. Особенность химии аминокислот и белков заключается в использовании многочисленных качественных (цветных) реакций, составлявших ранее основу химического анализа. В настоящее время, когда исследования проводятся с помощью физико-химических методов, многие качественные реакции продолжают применять для обнаружения α-аминокислот, например, в хроматографическом анализе.
Хелатообразование. С катионами тяжелых металлов α-аминокислоты как бифункциональные соединения образуют внутрикомплексные соли, например, со свежеприготовленным гидроксидом меди(11) в мягких условиях получаются хорошо кристаллизующиеся хелатные
соли меди(11) синего цвета (один из неспецифических способов обнаружения α-аминокислот).

Нингидринная реакция. Общая качественная реакция α-аминокислот - реакция с нингидрином. Продукт реакции имеет синефиолетовый цвет, что используется для визуального обнаружения аминокислот на хроматограммах (на бумаге, в тонком слое), а также для спектрофотометрического определения на аминокислотных анализаторах (продукт поглощает свет в области 550-570 нм).

Дезаминирование. В лабораторных условиях эта реакция осуществляется при действии азотистой кислоты на α-аминокислоты (см. 4.3). При этом образуется соответствующая α-гидроксикислота и выделяется газообразный азот, по объему которого судят о количестве вступившей в реакцию аминокислоты (метод Ван-Слайка).
Ксантопротеиновая реакция. Эта реакция используется для обнаружения ароматических и гетероциклических аминокислот - фенилаланина, тирозина, гистидина, триптофана. Например, при действии концентрированной азотной кислоты на тирозин образуется нитропроизводное, окрашенное в желтый цвет. В щелочной среде окраска становится оранжевой в связи с ионизацией фенольной гидроксильной группы и увеличением вклада аниона в сопряжение.

Существует также ряд частных реакций, позволяющих обнаруживать отдельные аминокислоты.
Триптофан обнаруживают при помощи реакции с п-(диметиламино)бензальдегидом в среде серной кислоты по появляющемуся красно-фиолетовому окрашиванию (реакция Эрлиха). Эта реакция используется для количественного анализа триптофана в продуктах расщепления белков.
Цистеин обнаруживают с помощью нескольких качественных реакций, основанных на реакционной способности содержащейся в нем меркаптогруппы. Например, при нагревании раствора белка с ацетатом свинца (СНзСОО)2РЬ в щелочной среде образуется черный осадок сульфида свинца PbS, что указывает на присутствие в белках цистеина.
12.1.5. Биологически важные химические реакции
В организме под действием различных ферментов осуществляется ряд важных химических превращений аминокислот. К таким пре- вращениям относятся трансаминирование, декарбоксилирование, элиминирование, альдольное расщепление, окислительное дезаминирование, окисление тиольных групп.
Трансаминирование является основным путем биосинтеза α-ами- нокислот из α-оксокислот. Донором аминогруппы служит аминокислота, имеющаяся в клетках в достаточном количестве или избытке, а ее акцептором - α-оксокислота. Аминокислота при этом превращается в оксокислоту, а оксокислота - в аминокислоту с соответствующим строением радикалов. В итоге трансаминирование представляет обратимый процесс взаимообмена амино- и оксо- групп. Пример такой реакции - получение l-глутаминовой кислоты из 2-оксоглутаровой кислоты. Донорной аминокислотой может служить, например, l-аспарагиновая кислота.

α-Аминокислоты содержат в α-положении к карбоксильной группе электроноакцепторную аминогруппу (точнее, протонированную аминогруппу NH 3 +), в связи с чем способны к декарбоксилированию.
Элиминирование свойственно аминокислотам, у которых в боковом радикале в β-положении к карбоксильной группе содержится электроноакцепторная функциональная группа, например гидроксильная или тиольная. Их отщепление приводит к промежуточным реакционноспособным α-енаминокислотам, легко переходящим в таутомерные иминокислоты (аналогия с кето-енольной таутомерией). α-Иминокислоты в результате гидратации по связи C=N и последующего отщепления молекулы аммиака превращаются в α-оксокислоты.

Такой тип превращений имеет название элиминирование-гидратация. Примером служит получение пировиноградной кислоты из серина.
Альдольное расщепление происходит в случае α-аминокислот, у которых в β-положении содержится гидроксильная группа. Например, серин расщепляется с образованием глицина и формальдегида (последний не выделяется в свободном виде, а сразу связывается с коферментом).
Окислительное дезаминирование может осуществляться с участием ферментов и кофермента НАД+ или НАДФ+ (см. 14.3). α-Аминокислоты могут превращаться в α-оксокислоты не только через трансаминирование, но и путем окислительного дезаминирования. Например, из l-глутаминовой кислоты образуется α-оксоглутаровая кислота. На первой стадии реакции осуществляется дегид- рирование (окисление) глутаминовой кислоты до α-иминоглутаровой
кислоты. На второй стадии происходит гидролиз, в результате которого получаются α-оксоглутаровая кислота и аммиак. Стадия гидролиза протекает без участия фермента.

В обратном направлении протекает реакция восстановительного аминирования α-оксокислот. Всегда содержащаяся в клетках α-оксоглутаровая кислота (как продукт метаболизма углеводов) превращается этим путем в L-глутаминовую кислоту.
Окисление тиольных групп лежит в основе взаимопревращений цистеиновых и цистиновых остатков, обеспечивающих ряд окислительно-восстановительных процессов в клетке. Цистеин, как и все тиолы (см. 4.1.2), легко окисляется с образованием дисульфида - цистина. Дисульфидная связь в цистине легко восстанавливается с образованием цистеина.

Благодаря способности тиольной группы к легкому окислению цистеин выполняет защитную функцию при воздействии на орга- низм веществ с высокой окислительной способностью. Кроме того, он был первым лекарственным средством, проявившим противолучевое действие. Цистеин используется в фармацевтической практике в качестве стабилизатора лекарственных препаратов.
Превращение цистеина в цистин приводит к образованию дисульфидных связей, например, в восстановленном глутатионе
(см. 12.2.3).
12.2. Первичная структура пептидов и белков
Условно считают, что пептиды содержат в молекуле до 100 (что соответствует молекулярной массе до 10 тыс.), а белки - более 100 аминокислотных остатков (молекулярная масса от 10 тыс. до нескольких миллионов).
В свою очередь, в группе пептидов принято различать олигопептиды (низкомолекулярные пептиды), содержащие в цепи не более 10 аминокислотных остатков, и полипептиды, в состав цепи которых входит до 100 аминокислотных остатков. Макромолекулы с числом аминокислотных остатков, приближающимся или немного превышающим 100, не разграничивают по понятиям полипептиды и белки, эти термины часто используют как синонимы.
Пептидную и белковую молекулу формально можно представить как продукт поликонденсации α-аминокислот, протекающей с обра- зованием пептидной (амидной) связи между мономерными звеньями (схема 12.2).
Конструкция полиамидной цепи одинакова для всего многообразия пептидов и белков. Эта цепь имеет неразветвленное строение и состоит из чередующихся пептидных (амидных) групп -СО-NH- и фрагментов -CH(R)-.
Один конец цепи, на котором находится аминокислота со свободной группой NH 2, называют N-концом, другой - С-концом,
Схема 12.2. Принцип построения пептидной цепи

на котором находится аминокислота со свободной группой СООН. Пептидные и белковые цепи записывают с N-конца.
12.2.1. Строение пептидной группы
В пептидной (амидной) группе -СО-NH- атом углерода находится в состоянии sp2-гибридизации. Неподеленная пара электронов атома азота вступает в сопряжение с π-электронами двойной связи С=О. С позиций электронного строения пептидная группа представляет собой трехцентровую p,π-сопряженную систему (см. 2.3.1), электронная плотность в которой смещена в сторону более электроотрицательного атома кислорода. Атомы С, Ои N, образующие сопряженную систему, находятся в одной плоскости. Распределение электронной плотности в амидной группе можно представить с по- мощью граничных структур (I) и (II) или смещения электронной плотности в результате +M- и - M-эффектов групп NH и C=O соответственно (III).

В результате сопряжения происходит некоторое выравнивание длин связей. Двойная связь С=О удлиняется до 0,124 нм против обычной длины 0,121 нм, а связь С-N становится короче - 0,132 нм по сравнению с 0,147 нм в обычном случае (рис. 12.1). Плоская сопряженная система в пептидной группе служит причиной затруднения вращения вокруг связи С-N (барьер вращения составляет 63-84 кДж/моль). Таким образом, электронное строение предопре- деляет достаточно жесткую плоскую структуру пептидной группы.
Как видно из рис. 12.1, α-атомы углерода аминокислотных остатков располагаются в плоскости пептидной группы по разные стороны от связи С-N, т. е. в более выгодном тpанс-положении: боковые радикалы R аминокислотных остатков в этом случае будут наиболее удалены друг от друга в пространстве.
Полипептидная цепь имеет удивительно однотипное строение и может быть представлена в виде ряда расположенных под углом друг

Рис. 12.1. Плоскостное расположение пептидной группы -CO-NH- и α-атомов углерода аминокислотных остатков
к другу плоскостей пептидных групп, соединенных между собой через α-атомы углерода связями Сα-N и Сα-Сsp 2 (рис. 12.2). Вращение вокруг этих одинарных связей весьма ограничено вследствие затруднений в пространственном размещении боковых радикалов аминокислотных остатков. Таким образом, электронное и пространственное строение пептидной группы во многом предопределяет структуру полипептидной цепи в целом.

Рис. 12.2. Взаимное положение плоскостей пептидных групп в полипептидной цепи
12.2.2. Состав и аминокислотная последовательность
При единообразно построенной полиамидной цепи специфичность пептидов и белков определяется двумя важнейшими характе- ристиками - аминокислотным составом и аминокислотной последовательностью.
Аминокислотный состав пептидов и белков - это природа и количественное соотношение входящих в них α-аминокислот.
Аминокислотный состав устанавливается путем анализа пептидных и белковых гидролизатов в основном хроматографическими методами. В настоящее время такой анализ осуществляется с помощью аминокислотных анализаторов.
Амидные связи способны гидролизоваться как в кислой, так и щелочной среде (см. 8.3.3). Пептиды и белки гидролизуются с образованием либо более коротких цепей - это так называемый частичный гидролиз, либо смеси аминокислот (в ионной форме) - полный гидролиз. Обычно гидролиз осуществляют в кислой среде, так как в условиях щелочного гидролиза многие аминокислоты неустойчивы. Следует отметить, что гидролизу подвергаются также амидные группы аспарагина и глутамина.

Первичная структура пептидов и белков - это аминокислотная последовательность, т. е. порядок чередования α-аминокислотных остатков.
Первичную структуру определяют путем последовательного отщепления аминокислот с какого-либо конца цепи и их идентификации.
12.2.3. Строение и номенклатура пептидов
Названия пептидов строят путем последовательного перечисления аминокислотных остатков, начиная с N-конца, с добавлением суффикса -ил, кроме последней С-концевой аминокислоты, для которой сохраняется ее полное название. Другими словами, названия
аминокислот, вступивших в образование пептидной связи за счет «своей» группы СООН, оканчиваются в названии пептида на -ил: аланил, валил и т. п. (для остатков аспарагиновой и глутаминовой кислот используют названия «аспартил» и «глутамил» соответствен- но). Названия и символы аминокислот означают их принадлежность к l -ряду, если не указано иное (d или dl ).

Иногда в сокращенной записи символами Н (как часть аминогруппы) и ОН (как часть карбоксильной группы) уточняется незамещенность функциональных групп концевых аминокислот. Этим способом удобно изображать функциональные производные пептидов; например, амид приведенного выше пептида по С-концевой аминокислоте записывается Н-Asn-Gly-Phe-NH2.
Пептиды содержатся во всех организмах. В отличие от белков они имеют более разнородный аминокислотный состав, в частнос- ти, довольно часто включают аминокислоты d -ряда. В структурном отношении они также более разнообразны: содержат циклические фрагменты, разветвленные цепи и т. д.
Один из наиболее распространенных представителей трипептидов - глутатион - содержится в организме всех животных, в растениях и бактериях.

Цистеин в составе глутатиона обусловливает возможность существования глутатиона как в восстановленной, так и окисленной форме.

Глутатион участвует в ряде окислительно-восстановительных процессов. Он выполняет функцию протектора белков, т. е. вещества, предохраняющего белки со свободными тиольными группами SH от окисления с образованием дисульфидных связей -S-S-. Это касается тех белков, для которых такой процесс нежелателен. Глутатион в этих случаях принимает на себя действие окислителя и таким образом «защищает» белок. При окислении глутатиона происходит межмолекулярное сшивание двух трипептидных фрагментов за счет дисульфидной связи. Процесс обратим.
12.3. Вторичная структура полипептидов и белков
Для высокомолекулярных полипептидов и белков наряду с первичной структурой характерны и более высокие уровни организа- ции, которые называют вторичной, третичной и четвертичной струк- турами.
Вторичная структура описывается пространственной ориентацией основной полипептидной цепи, третичная - трехмерной архитектурой всей белковой молекулы. Как вторичная, так и третичная структура связана с упорядоченным расположением макромолекулярной цепи в пространстве. Третичная и четвертичная структура белков рассматривается в курсе биохимии.
Расчетным путем было показано, что для полипептидной цепи одной из наиболее выгодных конформаций является расположение в пространстве в виде правозакрученной спирали, названной α-спиралью (рис. 12.3, а).
Пространственное расположение α-спирализованной полипептидной цепи можно представить, вообразив, что она обвивает некий

Рис. 12.3. α-Спиральная конформация полипептидной цепи
цилиндр (см. рис. 12.3, б). На один виток спирали в среднем приходится 3,6 аминокислотного остатка, шаг спирали составляет 0,54 нм, диаметр - 0,5 нм. Плоскости двух соседних пептидных групп располагаются при этом под углом 108?, а боковые радикалы аминокислот находятся на наружной стороне спирали, т. е. направлены как бы от поверхности цилиндра.
Основную роль в закреплении такой конформации цепи играют водородные связи, которые в α-спирали образуются между кар- бонильным атомом кислорода каждого первого и атомом водорода NН-группы каждого пятого аминокислотного остатка.

Водородные связи направлены почти параллельно оси α-спирали. Они удерживают цепь в закрученном состоянии.
Обычно белковые цепи спирализованы не полностью, а лишь частично. В таких белках, как миоглобин и гемоглобин, содержатся довольно длинные α-спиральные участки, например цепь миоглобина
спирализована на 75%. Во многих других белках доля спиральных участков в цепи может быть небольшой.
Другим видом вторичной структуры полипептидов и белков является β-структура, называемая также складчатым листом, или складчатым слоем. В складчатые листы укладываются вытянутые полипептидные цепи, связываемые множеством водородных связей между пептидными группами этих цепей (рис. 12.4). Во многих белках одновременно содержатся α-спиральные и β-складчатые структуры.

Рис. 12.4. Вторичная структура полипептидной цепи в виде складчатого листа (β-структура)
Основных аминокислот всего 20. Их названия связаны со случайными моментами. Все аминокислоты, которые входят в состав природных белков – это α -аминокислоты. Это значит, что амино- и карбоксильная группа находятся у одного углеродного атома.
1. аминоуксусная кислота (глицин);
2.  α-аминопропанова кислота (аланин);
α-аминопропанова кислота (аланин);
3.  α- аминопентановая кислота (валин);
α- аминопентановая кислота (валин);
4.  α-аминоизокапроновая кислота (лейцин);
α-аминоизокапроновая кислота (лейцин);
5.  α-амино-β-метилвалериановая кислота (изолейцин);
α-амино-β-метилвалериановая кислота (изолейцин);
6.  α-амино-β-гидроксипропановая кислота (серин);
α-амино-β-гидроксипропановая кислота (серин);
7.  α-амино-β-гидроксимасляная кислота (треонин);
α-амино-β-гидроксимасляная кислота (треонин);
Сера-содержащие :
8.  α-амино-β-меркаптопропановая кислота (цистеин);
α-амино-β-меркаптопропановая кислота (цистеин);
9.  α-амино-γ-метилтиомасляная кислота (метионин);
α-амино-γ-метилтиомасляная кислота (метионин);
10.  α-аминоянтарная кислота (аспарагиновая кислота);
α-аминоянтарная кислота (аспарагиновая кислота);
11.  амид аспарагиновой кислоты (аспарагин);
амид аспарагиновой кислоты (аспарагин);
12.  α-аминоглутаровая кислота (глутаминовая кислота);
α-аминоглутаровая кислота (глутаминовая кислота);
13.  амид α-аминоглутаровой кислоты (гутамин);
амид α-аминоглутаровой кислоты (гутамин);
14.  α, ε-диаминокапроновая кислота (лейзин);
α, ε-диаминокапроновая кислота (лейзин);
15.  α-амино-δ-гуанидиловалериановая кислота
α-амино-δ-гуанидиловалериановая кислота
(аргинин);
Циклические :
16.  α-амино-β-фенилпропановая кислота (фенилаланин);
α-амино-β-фенилпропановая кислота (фенилаланин);
17.  α-амино-β-пара-гидроксифенилпроавновая кислота (тирозин);
α-амино-β-пара-гидроксифенилпроавновая кислота (тирозин);
18.  α-амино-β-имидозолилпропановая ксилота (гистедин);
α-амино-β-имидозолилпропановая ксилота (гистедин);
19.  α-амино-β-индолилпропановая ксилота (триптофан);
α-амино-β-индолилпропановая ксилота (триптофан);
20.  α-тетрагидропироллкарбоновая кислота (пролин).
α-тетрагидропироллкарбоновая кислота (пролин).
Все природные аминокислоты относятся к L-стереохимическому ряду, D-рядя только как исключение у бактерий, в составе капсул, чтобы защитить бактерии от действия ферментов.
Лекция 3 .
Для каждой аминокислоты характерны свои единственные физико-химические свойства – изоэлектрическая точка, т.е. та pH среды, при которой раствор этой аминокислоты электронейтрален. (q = 0).
 Если же рассматривать такую кислоту в водной среде, то диссоциация происходит и по кислотному и по основному типу – биполярный ион.
Если же рассматривать такую кислоту в водной среде, то диссоциация происходит и по кислотному и по основному типу – биполярный ион.
В организме млекопитающих в печени имеется фермент оксидаза-D-аминокислот, который избирательно разрушает D-аминокислоты, которые попадают с продуктами питания. D-аминокислоты обнаружены в составе некоторых пептидов микроорганизмов. Кроме того, D-аминокислоты входят в состав большого числа антибиотиков. Например, D-валин, D-лейцин входят в состав антибиотика границидина, D-фенилаланин входит в состав границидина-С, пенициллин содержит необычный фрагмент D-диметилцистеин.
Процесс рацимизиации (переход D в L) происходит не ферментативно, поэтому очень медленно. На этом основано определение возраста млекопитающих.
 Все аминокислоты имеют в своем составе амино- и карбоксильную группу обладают свойствами аминов и карбоновых кислот. Кроме того, для α-аминокислот характерна нингидриновая реакция
(общая с белками). Со спиртовым раствором нингидрина очень быстро появляется сине-фиолетовая окраска, с пропином желтая.
Все аминокислоты имеют в своем составе амино- и карбоксильную группу обладают свойствами аминов и карбоновых кислот. Кроме того, для α-аминокислот характерна нингидриновая реакция
(общая с белками). Со спиртовым раствором нингидрина очень быстро появляется сине-фиолетовая окраска, с пропином желтая.

В конце XIX века была полемика, каким образом аминокислоты образуют связь если взять две аминокислоты, слить их вместе, то не получится никогда линейной структуры (в силу термодинамики, происходит циклизация). Получить полипептид в XIX веке никак не получалось.

Линейные молекулы никак не получатся. С т.з.термодинамики более выгодно отщепить 2Н 2 О, чем образовать линейную молекулу.
 В 1888 году химик Данилевский предположил, что белки – это полипептиды, линейные молекулы, которые образуются в результате действия карбоксильной группы одной аминокислоты с карбоксильной группой другой аминокислоты с отщеплением воды и образуется дипептид:
В 1888 году химик Данилевский предположил, что белки – это полипептиды, линейные молекулы, которые образуются в результате действия карбоксильной группы одной аминокислоты с карбоксильной группой другой аминокислоты с отщеплением воды и образуется дипептид:
 Образуется амидная связь (для белков пептидная), эти пептидные связи разделены только одним углеродным атомом. На основании биуретовой реакции
Данилевский сделал такой вывод. Это реакция раствора белка с сульфатом меди в щелочной среде, образуется сине-фиолетовое окрашивание, образуется хилатный комплекс с ионами меди, в результате того, что пептидная связь в белковых молекулах имеет специфическое строение. Вследствие кето-енольной таутомерии она на половину двойная, на половину одинарная. Характерная реакция с Cu(OH) 2:
Образуется амидная связь (для белков пептидная), эти пептидные связи разделены только одним углеродным атомом. На основании биуретовой реакции
Данилевский сделал такой вывод. Это реакция раствора белка с сульфатом меди в щелочной среде, образуется сине-фиолетовое окрашивание, образуется хилатный комплекс с ионами меди, в результате того, что пептидная связь в белковых молекулах имеет специфическое строение. Вследствие кето-енольной таутомерии она на половину двойная, на половину одинарная. Характерная реакция с Cu(OH) 2:
![]()
![]() Биуретовая реакция характерна для биурета (рис.1), для малонамида (рис.2) , белков.
Биуретовая реакция характерна для биурета (рис.1), для малонамида (рис.2) , белков.
Для того, чтобы окончательно доказать, что бели – это полипептиды в 1901 году Фишер синтезировал полипептид, независимо от него Гофман тоже синтезировал полипептид:
Синтез полипептида по Фишеру:

Продукт давал биуретовую реакцию, плохо растворялся, не обладал биологической активностью, расщеплялся протолитическими ферментами, а ферменты – это специфические биокатализаторы, которые расщеплют природные белки, значит у этого продукта такая же структура, как у природных белков.
В настоящее время синтезировано более 2 тысяч разных белков. Главное в синтезе белка – это защита аминогруппы и активация карбоксильной группы для того, чтобы синтез был направленным. Защита аминогрупп осуществляется ацилированием, для этого обрабатывают ангидридами трихлоруксусной кислоты и вводят трифторацильную группы, либо обрабатывают по Зенерсу (бензиловым эфиром хлоругольной кислоты).
Для синтеза каждого конкретного полипептида, для сшивания конкретного участка могут быть проведены свои собственные методы.
Защита по Зервесу , активация по Курциусу , снятие защиты по Бекману :

Твердофазный синтез полипептидов и белков, специфической особенностью полипептидного синтеза является огромное число однотипных операций. Был разработан метод Робертом Мерифилодм . Мономеры – это аминокислоты, которые используются для синтеза, содержащие защищенную аминогруппу и активированные карбоксильные группы – синтоны. Мерифилд предложил: первый мономер закрепить на полимерной смоле (нерастворимый носитель) и все последующие операции проводятся с полипептидом, растущем на полимерной основе, к смоле добавляют попеременно очередной синтон и реагент для удаления концевой защитной группы. Химические стадии перемежаются соответствующими промывками. В течение всего процесса полипептид остается связанным со смолой. Этот процесс легко можно автоматизировать, запрограммировав смену потоков через колонку. В настоящее время разработаны приборы синтезаторы. На завершающей стадии синтеза полипептид ковалентной связан со смолой, снимается с этой смолы и защитная группа удаляется. Одной из самых главных проблем в твердофазном синтезе является рацимизация аминокислот во время синтеза. Это особенно опасно в этом синтезе, т.к. промежуточных стадии выделения рациматов не существует. Способов отделения в данный момент не существует, но есть условия, чтобы как можно меньше была рацимизация. Сам Мерифилд получил этим методом сразу несколько полипептидов, был получен брадикидин – гормон с сосудорасширяющим действием, ангиотензин – гормон, повышающий кровяное давление, фермент рибонуклеаза, которая катализирует гидролиз РНК.
Выход продуктов этим методом значительно не сравним с методами, которые применялись до этого. С помощью автоматизации можно использовать этот метод в промышленных масштабах.
У каждого полипептида имеется N-конец, а другой С-конец. Аминокислота, которая принимает участие изменяет окончание на ил

Глицил-валил-тирозил-гистедин-аспарагил-пролин. Для определения аминокислот в полипептиде, необходимо провести гидролиз, его проводят при 100 С в течение 24 часов 6Н соляной кислотой. Далее продукты гидролиза анализируют – разделяют методом ионообменной хроматографии на колонке сульфалированным полистиролом. Потом вымывают цитратным буфером из колонки. По количеству элюента судят о том, какие кислоты, т.е. в начале будут вымываться кислые кислоты, а самыми последними – основные. Таким образом можно определять в какой момент, какая аминокислота прошла, а количество определяется фотометрически с помощью нингдрина, этим методом можно определить 1 мкг. Если необходимо оперделить 1 нг, применяют флуоросканин, он реагирует с α-аминокислотами, образуя сильно флуоросцилирующее соединение. Определяют какие и сколько аминокислот находятся, а последовательность аминокислот определить не удается.
Флюоросланин: